Ozempic se queda sin patente en la India y China, pero Europa tendrá que esperar: el mapa real de protección de la semaglutida | Negocios
La caducidad de la patente de la semaglutida —el principio activo de Ozempic y Wegovy— en países como la India, China o Canadá ha inaugurado la carrera para comercializar genéricos mucho más baratos, amenazando la mina de oro de Novo Nordisk. Sin embargo, la farmacéutica aún conserva la exclusiva en un gran número de países. Y es que la fecha límite del monopolio no es global. Mientras en India ya compiten por el negocio de los fármacos contra la diabetes (Ozempic) y la obesidad (Wegovy), en Europa o Estados Unidos los genéricos tendrán que esperar, al menos, hasta marzo y diciembre de 2031.
“La expiración de patentes forma parte del ciclo de vida natural de cualquier medicamento. Novo Nordisk está preparada para gestionar la pérdida de exclusividad de la semaglutida”, afirman fuentes de la compañía.
La cobertura de la semaglutida dibuja un mapamundi heterogéneo. En España, la protección de la patente caducará el 20 de marzo de 2031, el mismo día que en Alemania, Portugal, Italia, Suecia o Dinamarca, entre otros países europeos, así como en Japón y Australia. Tan solo un día después expirará en Grecia, mientras que en Francia, Reino Unido o Irlanda lo hará el 19 de marzo. En cambio, ya está liberada en Brasil o Turquía y también lo hará en México (7 de diciembre de 2027), Corea del Sur (5 de agosto de 2028) o Israel (23 de enero de 2029).
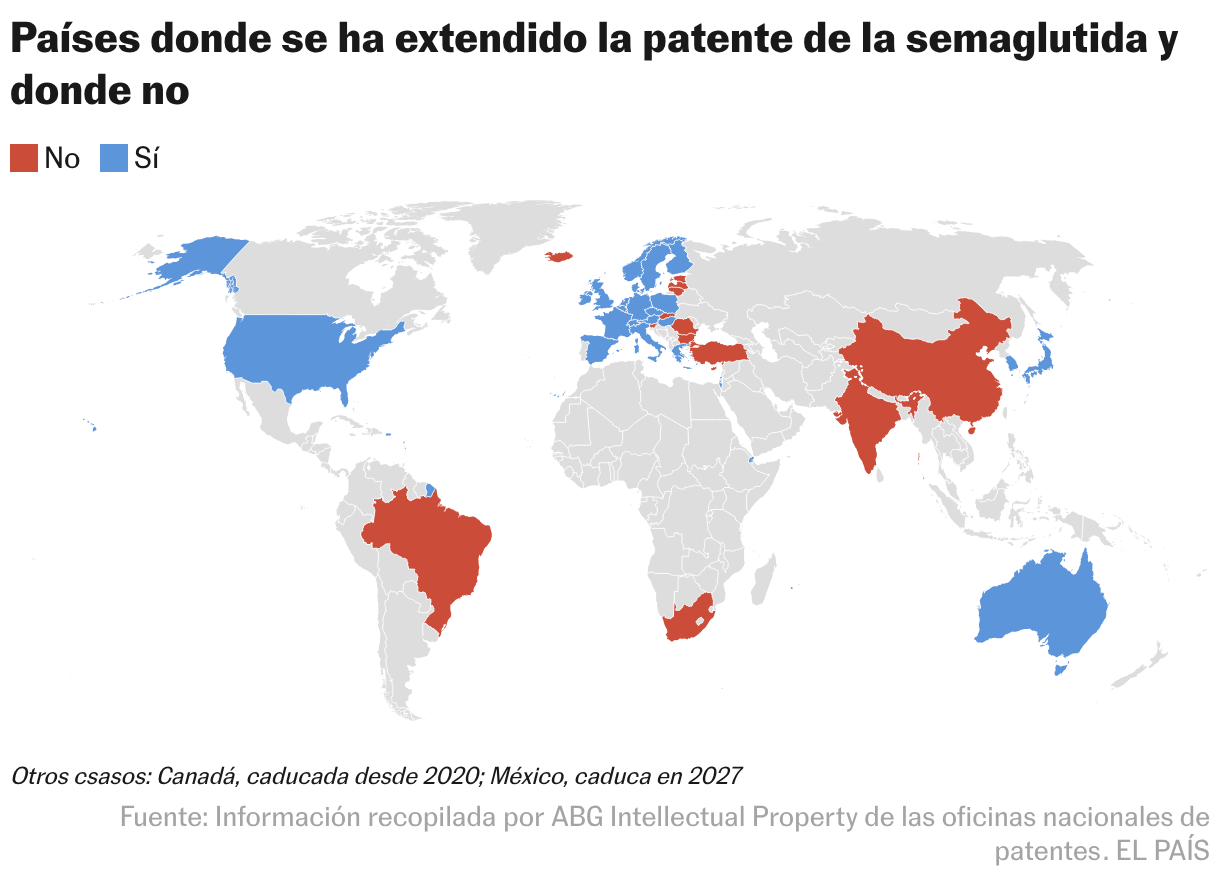
El baile de fechas tiene que ver con el juego de los distintos derechos de exclusividad, la legislación local y la estrategia de las farmacéuticas. “Todas las decisiones relacionadas con la propiedad intelectual se evalúan cuidadosamente a nivel global”, afirman desde Novo Nordisk. El caso de Canadá es paradigmático. La patente caducó en 2020 “debido al impago de las tasas de mantenimiento”, según Marta Rodríguez, socia en el departamento de patentes químicas y farmacéuticas de ABG IP. Sin embargo, su exclusividad regulatoria finalizó el 4 de enero de 2026, confirma la farmacéutica. “Actualmente, Novo Nordisk es la única compañía con productos aprobados por Health Canada que contienen semaglutida”, declara.
La patente tiene una duración de 20 años desde la fecha de la solicitud en la inmensa mayoría de países. Pero no es oro todo lo que reluce: “Se necesitan unos 10 años de media para completar los ensayos clínicos y los procedimientos regulatorios para obtener la autorización de comercialización de un medicamento”, señala Rodríguez. Por este motivo, se han creado mecanismos compensatorios que alargan la protección efectiva de esta inversión millonaria. Ahí es cuando se complican las cuentas.
En la UE esta extensión se denomina certificado complementario de protección (CCP), un título jurídico que creó la Comisión en los años 90 “para prorrogar hasta un máximo de cinco años la protección del producto”, cuenta Miquel Montañá, socio de Clifford Chance especializado en litigios sobre patentes. La duración concreta depende de lo que haya tardado el laboratorio en obtener la autorización de comercialización. En el caso de la semaglutida, como se retrasó 10 años o más desde la presentación de la patente, se ha añadido el máximo: cinco años.
La concesión de este certificado es vital para un blockbuster como el Ozempic. Según el informe 2025 de Novo Nordisk, sus ventas aumentaron un 6% en coronas danesas y un 10% a tipo de cambio constante, alcanzando los 127.089 millones de coronas (más de 17.000 millones de euros). Eso sí, “la obtención de un CCP no es automática ni está unificada”, advierte Rodríguez. Esto significa “que Novo Nordisk tiene que solicitar el certificado país por país” y que “puede haber variaciones en su aplicación”. Si miramos más allá del Viejo Continente, el rompecabezas está servido: “En EE UU, China o Israel sí disponen de estas extensiones, aunque cada país define sus requisitos y duración, mientras que en India o Brasil no existe este tipo de herramienta”.
En algunos Estados existe un blindaje adicional que impide la comercialización de genéricos durante 10 años. “La protección de datos de registro permite un verdadero monopolio inexpugnable y es muy útil cuando no hay patente”, afirma Manuel Lobato, of counsel del departamento de propiedad industrial e intelectual de Bird & Bird. Este fue el caso del paclitaxel (Taxol), el tratamiento base del cáncer de mama: como era conocido desde la II Guerra Mundial “lo único que podía protegerse eran los datos de registro”. Una vez que expira el plazo, las empresas de genéricos “pueden apoyarse en los datos de los innovadores para obtener una autorización de los medicamentos simplificada” y evitar ensayos innecesarios.
La complejidad es aún mayor: las distintas capas de protección de un medicamento pueden llegar a conformar una auténtica maraña jurídica. Además de la patente principal de la semaglutida en Europa —EP 1863839 B1, presentada el 20 de marzo de 2006— Novo Nordisk dispone de una amplia cartera de patentes secundarias dirigidas, por ejemplo, a su uso en determinadas dosis o las vías de administración o nuevas aplicaciones médicas.
Equilibrio
Las tácticas para extender la vida comercial de la patente —conocidas como evergreening— caminan en un alambre entre el incentivo a la innovación y la competencia. Elena Casaus, secretaria general de la Asociación Española de Medicamentos Genéricos (AESEG), denuncia que no siempre existe equilibrio: “Un estudio reciente de International Generic and Biosimilar Medicines Association demuestra cómo algunas compañías recurren a estrategias de evergreening que pueden prolongar artificialmente su monopolio más allá de la protección legítima”. Estas prácticas, añade, encarecen los litigios —superan los 10 millones de dólares en los mercados principales— y “retrasan la entrada de alternativas más asequibles”.
Las compañías de genéricos juegan sus cartas para derribar barreras. Por ejemplo, una vigilancia activa permite presentar observaciones ante las oficinas de patentes. “Muchas veces de manera anónima o mediante hombres de paja”, comenta Miquel Montañá. En fase administrativa actúan principalmente los agentes; los tribunales quedan, por lo general, en manos de abogados. El resultado de estos rifirrafes no está escrito en piedra: “Es habitual que una misma patente se mantenga en unos países y se revoque en otros”, señala. Un ejemplo reciente es el caso del apixabán (Eliquis) un medicamento anticoagulante, cuya patente fue revocada hace tres años en el Reino Unido. En España, al igual que en el resto de países de Europa continental donde se impugnó, el Tribunal Supremo confirmó su validez en abril de 2025.
Niños obesos
Uno de cada cinco niños en edad escolar tiene obesidad o sobrepeso. Para 2040, un total de 507 millones de menores convivirán con esta patología, según el Atlas Mundial de la Obesidad 2026. Wegovy no puede usarse aún en los más pequeños al no estar recomendado para menores de 12 años. Sin embargo, Novo Nordisk está investigando la seguridad y la eficacia de semaglutida en esta población, para lo que han puesto en marcha el estudio clínico Step Young. “Los posibles pasos futuros y eventuales indicaciones dependerán de los resultados de los estudios, de la evaluación de las autoridades regulatorias y de las decisiones que se adopten conforme a los marcos regulatorios aplicables”, afirma la compañía. La UE permite ampliar seis meses la exclusividad en el mercado si se completa un plan de investigación pediátrica aprobado por la Agencia Europea del Medicamento.

